Инновации в лечении бета-талассемии: фокус на патогенетическую терапию
Профиль пациента, который может выиграть от назначения инновационной терапии бета-талассемии, разобрали Наталия Сергеевна Сметанина, д.м.н., профессор, зам. генерального директора - директор управления по планированию и стратегическому развитию службы детской онкологии и гематологии, врач-гематолог ФГБУ «НМИЦ ДГОИ им. Дмитрия Рогачева» Минздрава России и Родион Викторович Пономарев, к.м.н., руководитель сектора изучения неопухолевых заболеваний системы крови, врач-гематолог отделения гематологии и химиотерапии орфанных заболеваний ФГБУ НМИЦ гематологии Минздрава России. Эксперты поделились опытом использования инновационных препаратов для лечения маленьких и взрослых пациентов.
Понятия
Бета-талассемия — это моногенное заболевание вследствие количественного нарушения синтеза бета-глобиновых цепей. В результате этого дисбаланса глобиновых цепей, развивается неэффективный эритропоэз, когда количество делящихся предшественников- эритроцитов огромное количество, а клеток, которые выходят в конечную дифференцировку и становятся зрелыми эритроцитами, катастрофически мало.
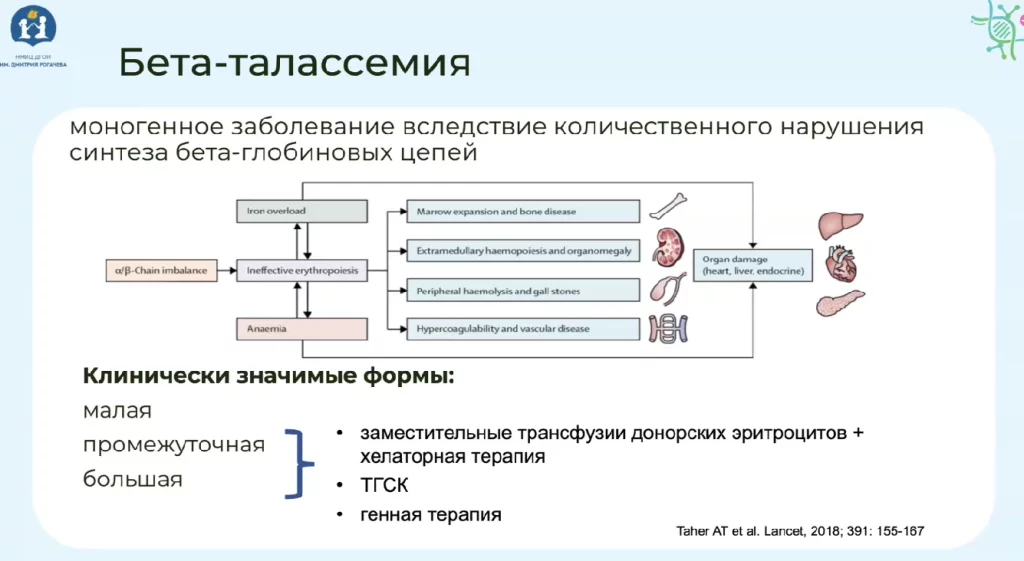
В результате этого у пациентов развивается анемия и складываются условия для развития перегрузки железом, как вследствие акселерированного эритропоэза и анемии, так и вследствие проводимого лечения для пациентов с тяжелыми формами.
Сам по себе неэффективный эритропоэз, если не оказывать пациенту какого-либо лечения, также имеет множество тяжелых последствий:
- выход кроветворных масс за пределы костной ткани с формированием экстрамедуллярного гемопоэза,
- выход кроветворения в печень, селезенку,
- внутрисосудистый гемолиз,
- усиленное образование конкрементов в желчном пузыре,
- это создает условия гиперкоагуляции,
- риски тромботических осложнений.
Формы патологии
Клинически выделяют формы:
- малую,
- промежуточную,
- большую.
Промежуточная и большая формы требуют пристального внимания и активного лечения.
На рисунке ниже представлена гистологическая картина возврата гемопоэза, а именно эритропоэза в ткань селезенки.
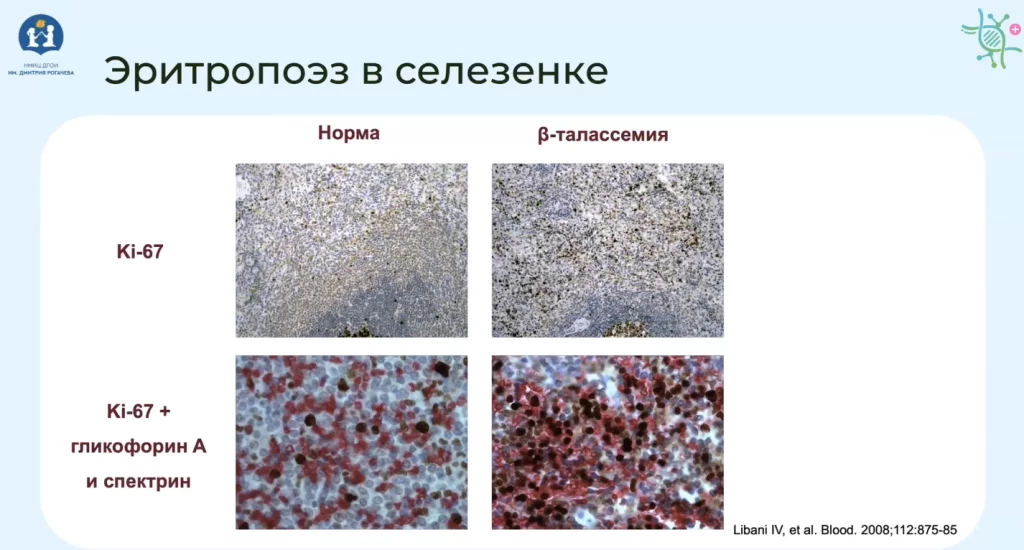
В данном случае при бета-талассемии после удаления селезенки проведено гистологическое исследование, и видно насколько интенсивно фиксируются у пациентов с талассемией ранние предшественники эритропоэза в ткани селезенки, что подтверждает его возврат.
Аналогичная картина происходит и в печени.
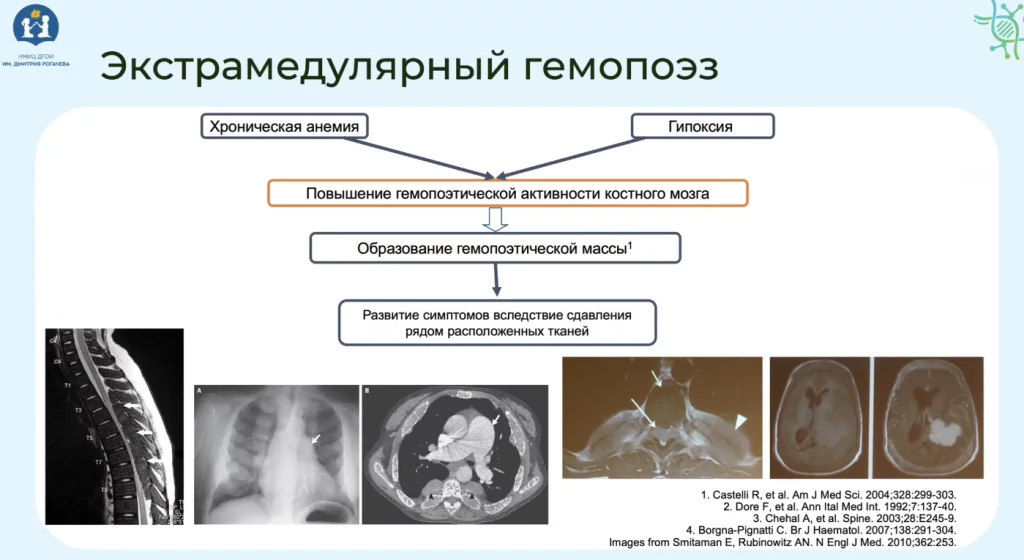
Если не оказать адекватного лечения, то возникает так называемый экстрамедулярный гемопоэз, который может сдавливать спинной мозг. На рисунке выше видны кроветворные массы, вышедшие за пределы плоских костей, остистых отростков позвонков, фактически передавливающие спинной мозг.
Это фактически жизнеугрожающие вещи. И именно предотвращение появления экстрамедулярного гемопоэза и ограничение темпов кроветворения, а лучше — прекращение кроветворения в печени и селезенке — это цель любой терапии бета-талассемии промежуточной и тяжёлой формы.
Что можно предложить пациентам?
- Заместительные трансфузии донорских эритроцитов в сопровождении хелаторной терапии,
- Для ограниченного числа пациентов трансплантации гемопоэтических стволовых клеток, то есть радикальной терапии.
В мире существуют генные терапии, но пока в нашей стране нет к ним доступа.
Но можно проводить радикальную терапию в объеме классической трансплантации гемопоэтических стволовых клеток, что на сегодня уже доказано для пациентов с промежуточной большой формы бета-таллицемии.
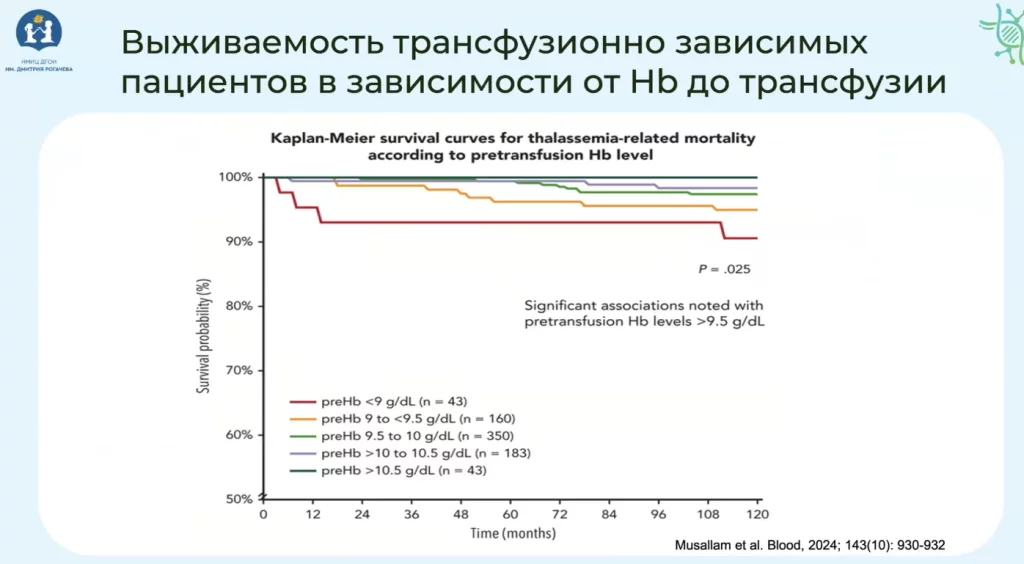
Оказалось, что если до регулярной трансфузии гемоглобин у пациента опускается менее 95 г/л, то глобальная его продолжительность жизни сокращается фактически на 10% относительно общепопуляционной.
Важно! Именно за счет того, что акселерируется эритропоэз в печени и селезенке усиливается интенсивность прокоагуляции и, соответственно, могут развиться многочисленные осложнения.
Поэтому очень важно выполнять наши национальные клинические рекомендации, которые полностью согласуются с рекомендациями Всемирной Талассимической Федерации по ведению пациентов с трансфузионно-зависимой большой формой.
Осложнения при недолжном лечении
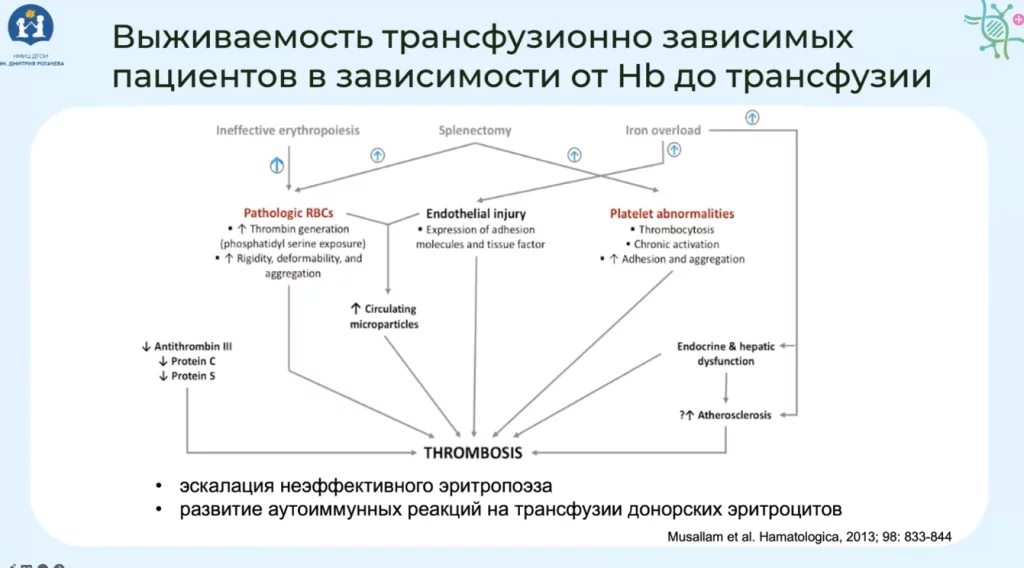
Именно за счет неэффективного эритропоэза, который сопровождает данное заболевание, происходит повреждение эндотелия сосудов. Он способствует изменению адгезии и агрегации тромбоцитов, и именно за счет патологически измененных эритроцитов, циркулирующих в кровотоке, появляется дополнительное количество микровизикул, которые обладают также протравматическими свойствами.
В итоге у пациентов, если они не получают неадекватное лечение и имеют весьма активный неэффективный эритропоэз, развиваются всевозможные травматические осложнения во взрослом возрасте.
У педиатрических пациентов таких осложнений пока не наблюдают, но видны уже выраженные проявления неэффективного эритропоэза за счет гигантской гепатомегалии, спленомегалии.
У части пациентов уже к 12 годам при невыполнении национальных клинических рекомендаций можно увидеть, и врачи вынуждены проводить агрессивное лечение экстрамедулярных масс вдоль позвоночника.
Аутоимунные реакции
Следующее неприятное осложнение — аутоиммунные реакции на трансфузии донорских эритроцитов.
Это осложнение может развиться вследствие:
- редких трансфузий, и патологически измененные эритроциты могут провоцировать развитие аутоиммунных реакций на донорские эритроциты.
- трансфузии пациентам с промежуточной формой бета-таллосемии и при неправильно подобранных донорских эритроцитов. Если по минорным группам, например, не совпало, то у пациентов может развиться также аутоиммунный гемолиз и в том числе у пациентов с большой формой β-толосемии.
И также у детей наблюдается развитие так называемого синдрома гипергемолиза, обусловленного гиперактивацией макрофагов, что является жизнеугрожающим осложнением у данной категории пациентов.
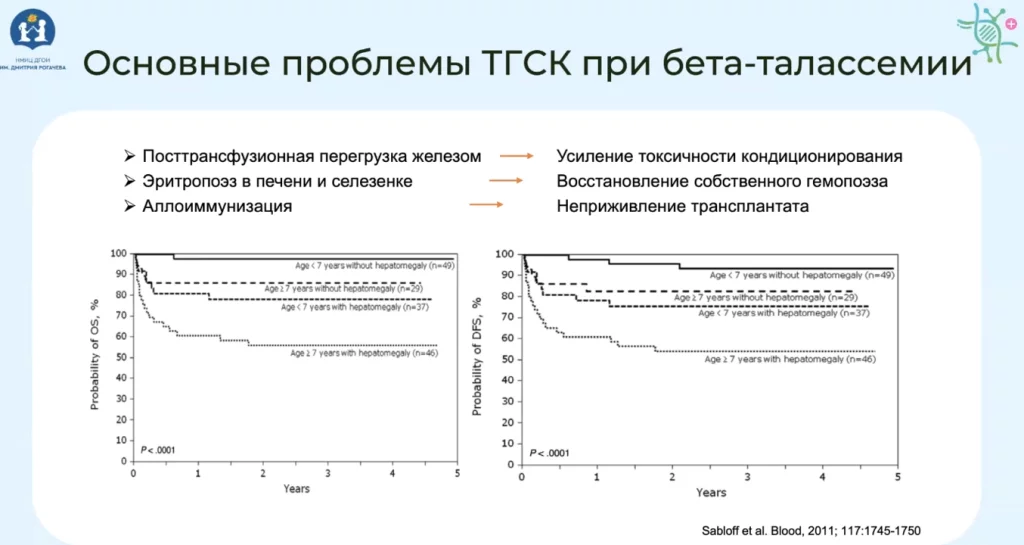
Если посмотреть на результаты радикальной терапии, то отсутствие эритропоэза в печени и селезенке принципиально, поскольку если у пациента есть органы мегалия, соответственно там есть собственный эритропоэз, то крайне высоки риски восстановления собственного талласимического гемопоэза после трансплантации гемопоэтических стволовых клеток.
Если случилась аллоиммунизация вследствие многочисленных трансфузий, то возможно не приживление трансплантата.
Возрастные особенности у детейВажно! Все это глобально ухудшает выживаемость при радикальной терапии бета-талассемии.
Если посмотреть на общую выживаемость пациентов младше 7 лет, с отсутствием гепатоспленомегалии, то это примерно 98%.
Выживаемость без заболевания составляет 95 процентов. Это колоссальный успех, и такие же результаты даются и в нашей стране.
Если пациент старше 7 лет и имеет гепатоспленомегалию, то результаты уже в половину хуже, как общая выживаемость, так и выживаемость без талассемии. Это подчеркивает в очередной раз важность правильного ведения талассемиков и возможность использования всех современных лекарственных препаратов для того, чтобы ограничить неэффективный эритропоэз и сохранить пациенту возможность радикальной терапии.
Более подробно о препаратах и алгоритмах лечения детей и взрослых смотрите в видеолекции экспертов.